Forskere ved Scripps Research Institute har avdekket en skjult arkitektur inne i cellenes mystiske væskedråper. Funnet snur opp-ned på et grunnleggende bilde av hvordan celler er organisert – og åpner for nye angrepspunkter mot kreft og ALS. Studien ble publisert i Nature Structural and Molecular Biology den 2. februar 2026.
Der forskere før så ustrukturerte dråper, ser de nå komplekse nettverk av proteinfilamenter som styrer hvordan dråpene fungerer.
Hva er oppdaget?
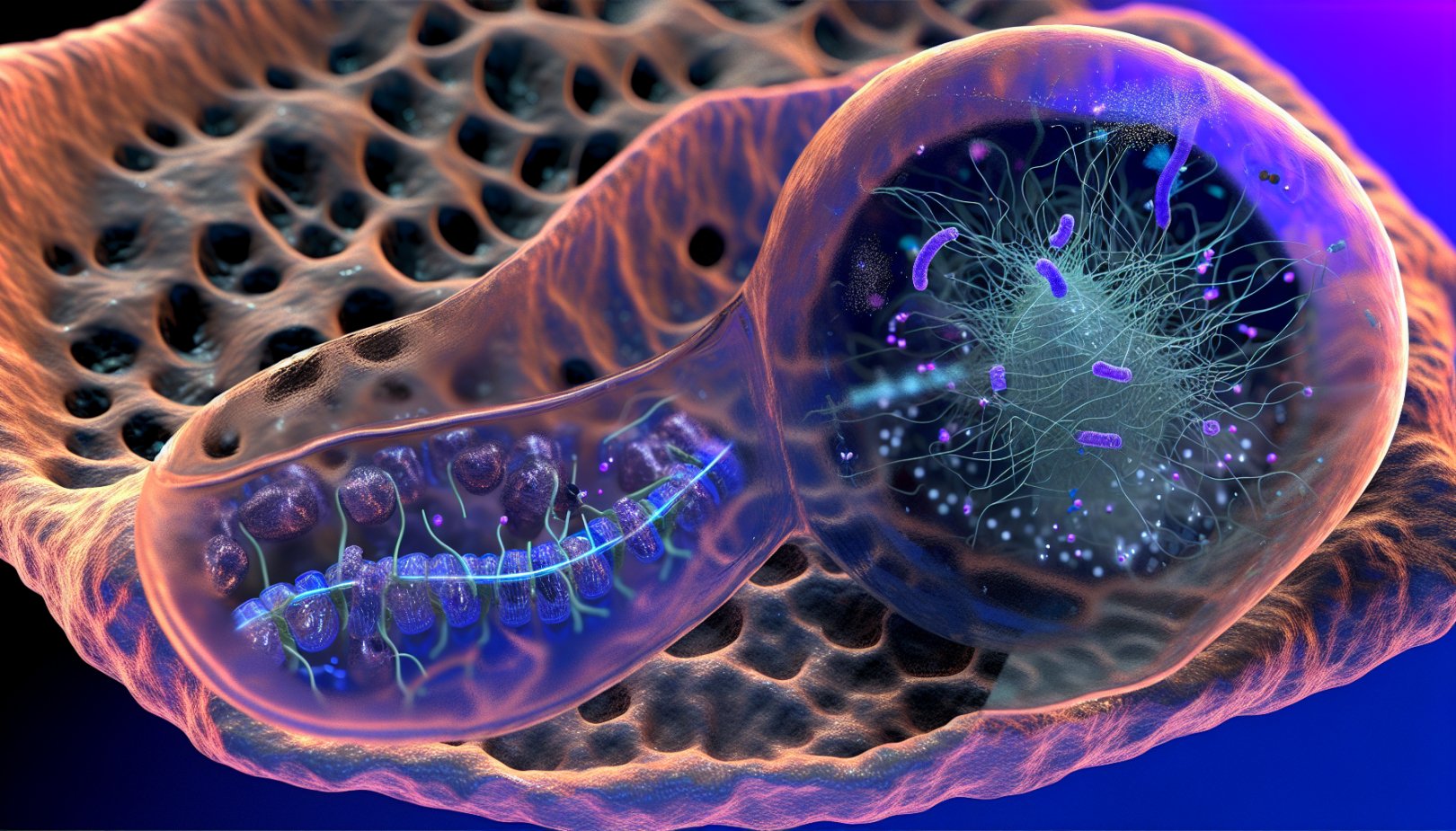
Teamet ledet av professor Keren Lasker, sammen med professor Ashok Deniz og assisterende professor Raphael Park, viser at noen biomolekylære kondensater i celler er bygget opp av tynne, trådlignende filamenter. Disse danner et indre stillas som gir dråpene en definert struktur – avgjørende for funksjon.
Dråpelignende ansamlinger av proteiner og andre biomolekyler uten membran. De kan smelte sammen, flyte og raskt bytte komponenter, og er sentrale for blant annet genregulering og opprydding av celleavfall.
Slik gjorde de det
Forskerne studerte et bakterieprotein kalt PopZ, som samler seg ved cellens poler og danner kondensater som organiserer andre proteiner nødvendige for celledeling.
- Ved hjelp av kryo-elektronmikroskopi (cryo-ET) – som fungerer som en CT-skanning på molekylært nivå – viste de at PopZ settes sammen i filamenter gjennom en ordnet, trinnvis prosess.
- Filamentene danner et stillas som bestemmer kondensatenes fysiske egenskaper.
- Med enkeltmolekyl-FRET, som måler svært små avstander i proteiner, fant de at PopZ endrer form avhengig av om det er utenfor eller inne i kondensatet.
Hva skjer når stillaset bryter sammen?
For å teste betydningen av filamentene, konstruerte teamet en mutert PopZ-variant som ikke kunne danne filamenter.
- Kondensatene ble mye mer flytende og fikk lavere overflatespenning.
- I levende bakterier stoppet cellene å vokse og klarte ikke å dele DNA ordentlig.
Konklusjonen: Fysiske egenskaper ved kondensatet, ikke bare de kjemiske komponentene, er kritiske for normal cellefunksjon.
Hvorfor betyr dette noe for sykdom?
I menneskelige celler har filamentbaserte kondensater to hovedoppgaver:
- Fjerne skadede eller giftige proteiner – svikt her kan føre til opphopning av skadelige proteiner, et kjennetegn ved nevrodegenerative sykdommer som ALS.
- Kontrollere cellevekst – svikt kan kollapse beskyttende mekanismer mot svulster og bidra til kreft, inkludert prostata-, bryst- og livmorkreft.
«Helt siden vi innså at forstyrrelser i kondensatdannelse står sentralt i mange sykdommer, har det vært utfordrende å målrette dem terapeutisk fordi de så ut til å mangle struktur – det fantes ingen spesifikke trekk for et medikament å feste seg til,» sier Lasker. «Dette arbeidet endrer det. Vi kan nå se at noen kondensater har en indre arkitektur, og at denne strukturen er nødvendig for funksjon.»
Et nytt medisinsk mål
Ved å demonstrere at kondensatarkitektur både kan defineres og er funksjonelt kritisk, åpner funnene for terapier som retter seg mot struktur – med mål om å korrigere den underliggende disorganiseringen som gir sykdom fotfeste.
Studien er publisert i Nature Structural and Molecular Biology den 2. februar 2026. Daniel Scholl, tidligere postdoktor i Lasker- og Deniz-laboratoriene, er førsteforfatter. Prosjektet er støttet av flere avdelinger ved National Institutes of Health, National Science Foundation og andre forskningsorganisasjoner.
Nøkkelfunn i kortform
- Filamenter danner et indre stillas i noen kondensater og styrer deres egenskaper.
- PopZ skifter form avhengig av om det er utenfor eller inne i kondensatet.
- Manglende filamenter gjør kondensater mer flytende og senker overflatespenningen.
- I bakterier gir dette stopp i vekst og feil i DNA-segregering.
- Funnene er relevante for ALS og kreft (prostata, bryst, livmor) der kondensatfunksjon er avgjørende.
Hovedpoenget: Oppdagelsen markerer et paradigmeskifte i forståelsen av cellulær organisering. Der ustrukturerte dråper ble antatt å være normen, avdekkes nå funksjonelle arkitekturer med potensial som mål for nye behandlinger.
Kilder: ScienceDaily, Phys.org, EurekAlert!, News-Medical.net, Nature Structural and Molecular Biology






Kommentarer
0 kommentarer
Vi godtar kun kommentarer fra registrerte brukere. Dette gjør vi for å opprettholde en trygg og respektfull debatt, samt for å unngå spam og misbruk. Registrering er gratis og tar bare noen sekunder.
Du må være innlogget for å kommentere. Logg inn eller registrer deg for å delta i diskusjonen.